Das Elektrodenpotential ist der Unterschiedelektrostatische Potentiale zwischen dem Elektrolyten und der Elektrode. Die Entstehung eines solchen Potentials ist auf die räumliche Trennung von Ladungen zurückzuführen, die entgegengesetzte Vorzeichen an der Phasentrenngrenze haben, wobei sich eine elektrische Doppelschicht bildet.
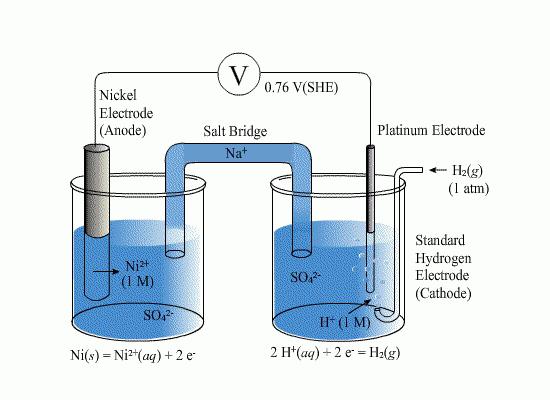
Räumliche Ladungstrennung an der Grenzezwischen der Metallelektrode und der Elektrolytlösung durch solche Phänomene wie die Übertragung der Metallionen in Lösung in dem Verfahren zur Herstellung eines elektrochemischen Gleichgewichts und der Adsorption von Ionen aus dem Elektrolyten an der Elektrodenoberfläche zur Festlegung; Verdrängung von Gas über das positiv geladene Ionengitter hinaus; Noncoulomb-Adsorption von Ionen oder Molekülen einer Flüssigkeit auf einer Elektrode. Aufgrund der letzten beiden Phänomene ist das Elektrodenpotential niemals Null, selbst wenn die Ladung der Metalloberfläche Null ist. Der absolute Wert des Potentials einer einzelnen Elektrode ist nicht für dieses Verfahren definiert wird, um den Vergleich der Referenz- und Testelektroden verwendet. Das Elektrodenpotential ist gleich die Größe der elektromotorischen Kraft (EMF), in der elektrochemischen Schaltung erhalten.

Für Lösungen auf WasserbasisVerwenden Sie Wasserstoffelektroden. Standardelemente dieser Art werden als Standards für eine Vielzahl von elektrochemischen Messungen sowie in galvanischen Vorrichtungen verwendet. Eine Wasserstoffelektrode ist ein Draht oder eine Metallplatte, die gasförmigen Wasserstoff gut absorbiert (häufig wird Palladium oder Platin verwendet). Eine solche Drahtplatte wird bei Atmosphärendruck mit Wasserstoff gesättigt, wonach sie in eine wässrige Lösung eingetaucht wird, die reich an Wasserstoffionen ist. Das Potential einer solchen Platte ist proportional zur Konzentration von Ionen in der Lösung. Das Element ist der Standard, relativ dazu wird das Elektrodenpotential der chemischen Reaktion gezählt.
Bei der Montage von galvanischen Zellen auf der BasisWasserstoff und detektierbare Vorrichtungen findet auf der Oberfläche des Metalls der Platingruppe eine Reaktion (reversibel) statt, was entweder den Reduktions- oder den Oxidationsprozess bedeutet. Die Art des Prozesses hängt von dem Potential der Reaktion des zu bestimmenden Elements ab. Wasserstoffelektrodenpotential bestimmt wird, Null zu sein, wenn der Wasserstoffdruck etwa eine Atmosphäre, die Protonenkonzentration der Lösung - ein Mol pro Liter und die Temperatur - 298 K. Wenn das analysierte Element in den Referenzbedingungen, das heißt, wenn die Ionenaktivität, die Kapazität der Anlage zu beeinträchtigen, und der Gasdruck beträgt 0,101 MPa, der Wert dieses Potentials wird als Standard bezeichnet.
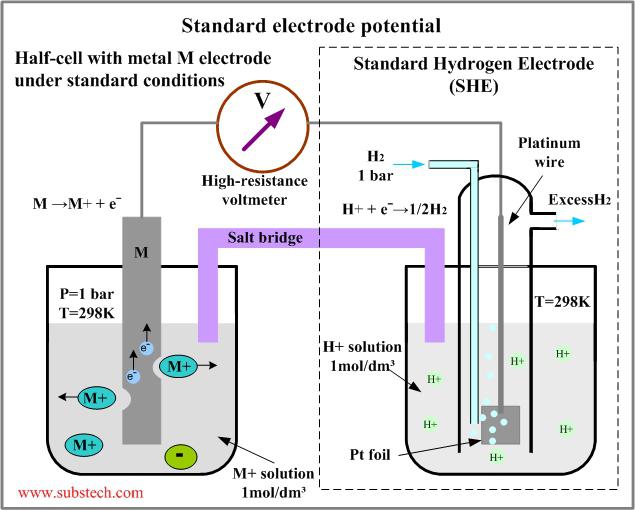
Messung der EMF einer galvanischen Elektrode inStandardbedingungen wird das Standardelektrodenpotential der chemischen Reaktion berechnet. Üblicherweise wird dieser Wert unter Bedingungen gemessen, bei denen alle thermodynamischen Aktivitäten der potentialbestimmenden Reaktion gleich eins sind und der Gasdruck 0,01 * 105 Pa beträgt. Das Potential des zu prüfenden Elements wird als positiv angesehen, wenn sich im externen Stromkreis im "Stromquellen" -Modus Elektronen von links nach rechts und positiv geladene Teilchen im Elektrolyten bewegen.