Wie findet ein Stoffübergang von einem flüssigen in einen festen Zustand statt?
Jede Veränderung des Aggregatzustands ist mit der Metamorphose von Temperatur und Druck verbunden. Ein Stoff kann in folgenden Aggregatzuständen dargestellt werden: fest, flüssig, gasförmig.
Wir bemerken, dass der Übergang nicht beobachtet wirdVeränderungen in der Zusammensetzung der Materie. Der Übergang der Materie vom flüssigen Zustand in den festen Zustand ist nur von einer Änderung der Kräfte der intermolekularen Wechselwirkung, der Anordnung der Moleküle begleitet. Die Umwandlung von einem Zustand in einen anderen wird als Phasenübergang bezeichnet.

Schmelzen
Dieser Prozess beinhaltet die Umwandlung eines Feststoffes in eine Flüssigkeit. Es erfordert eine erhöhte Temperatur.
Zum Beispiel können Sie in der Natur beobachten wieZustand der Substanz. Die Physik erklärt leicht das Schmelzen von Schneeflocken unter dem Einfluss von Frühlingsstrahlen. Die kleinen Eiskristalle, die Teil des Schnees sind, brechen nach dem Erhitzen der Luft auf Null ab. Das Schmelzen erfolgt allmählich. Erstens nimmt Eis Wärmeenergie auf. Wenn sich die Temperatur ändert, verwandelt sich das Eis vollständig in flüssiges Wasser.
Es ist begleitet von einer signifikanten Erhöhung der Geschwindigkeit der Teilchenbewegung, thermische Energie, eine Erhöhung des Wertes der inneren Energie.
Nach dem Erreichen des Indikators, aufgerufenSchmelztemperatur ist die Struktur eines Festkörpers gebrochen. Moleküle haben größere Freiheit, sie "springen" und besetzen unterschiedliche Positionen. Die geschmolzene Substanz hat eine größere Energiereserve als im festen Zustand.
Härtungstemperatur
Der Übergang einer Substanz von einem flüssigen Zustand in einen festen Zustand tritt bei einer bestimmten Temperatur auf. Wenn dem Körper Wärme entzogen wird, gefriert er (kristallisiert).
Die Erstarrungstemperatur wird als eine der wichtigsten Eigenschaften angesehen.
Kristallisation
Der Übergang der Materie vom flüssigen zum festen ZustandPosition heißt Kristallisation. Wenn die Wärmeübertragung von der Flüssigkeit aufhört, fällt die Temperatur auf einen bestimmten Wert ab. Der Phasenübergang einer Substanz von einem flüssigen Zustand zu einem Festkörper in der Physik wird Kristallisation genannt. Bei Betrachtung einer Substanz, die keine Verunreinigungen enthält, entspricht die Schmelztemperatur dem Kristallisationsindex.
Beide Prozesse verlaufen schrittweise. Der Kristallisationsprozess geht mit einer Abnahme der mittleren kinetischen Energie der in der Flüssigkeit enthaltenen Moleküle einher. Die Anziehungskräfte, durch die die Teilchen in einer festen Reihenfolge gehalten werden, die den Festkörpern eigen ist, nehmen zu. Nachdem die Partikel eine geordnete Anordnung erhalten haben, wird ein Kristall gebildet.
Ein Aggregatzustand ist eine physische FormSubstanz, in einem bestimmten Bereich von Drücken und Temperaturen dargestellt. Es ist durch quantitative Eigenschaften gekennzeichnet, die in ausgewählten Intervallen geändert werden:
- die Fähigkeit einer Substanz, Form und Volumen zu verändern;
- Abwesenheit (Anwesenheit) von Fern- oder Nahbereich.
Der Prozess der Kristallisation ist mit Entropie, freier Energie, Dichte und anderen physikalischen Größen verbunden.
Neben Flüssigkeiten, Feststoffen, gasförmigen Formen entsteht ein weiterer Aggregatzustand - Plasma. Es kann im Falle einer Temperaturerhöhung bei konstantem Druck in Gase umgewandelt werden.
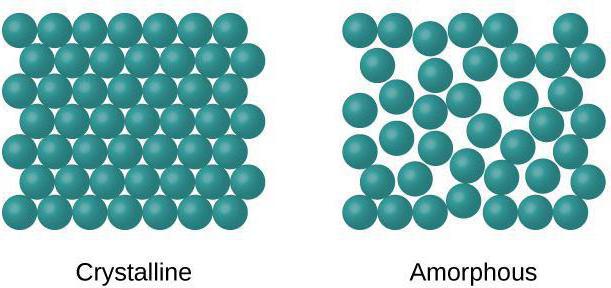
Der Rahmen zwischen den verschiedenen Aggregatzuständenweit davon entfernt, immer streng zu sein. In der Physik wurde die Existenz amorpher Körper bestätigt, die in der Lage sind, die Struktur einer Flüssigkeit mit einer geringen Fluidität beizubehalten. Flüssigkristalle haben die Fähigkeit, elektromagnetische Strahlung, die durch sie hindurchgeht, zu polarisieren.

Fazit
Um die verschiedenen Zustände in. Zu beschreibenPhysik, wenden Sie die Definition der thermodynamischen Phase an. Kritische Phänomene heißen Zustände, die die Umwandlung einer Phase in eine andere beschreiben. Feststoffe unterscheiden sich durch Konservierung über einen langen Zeitraum ihrer durchschnittlichen Position. Sie werden geringe Schwankungen (mit einer minimalen Amplitude) in der Nähe der Gleichgewichtsposition machen. Kristalle haben eine bestimmte Form, die sich beim Übergang in den flüssigen Zustand ändert. Informationen über den Siedepunkt (Schmelzen) erlauben Physikern, Übergänge von einem Aggregatzustand zu einem anderen für praktische Zwecke zu verwenden.