Grundlegende MKT-Gleichung und Temperaturmessung
Die Untersuchung von Prozessen in statistischenSysteme, ist durch die minimale Größe von Partikeln und eine große Anzahl von ihnen kompliziert. Es ist praktisch unmöglich, jedes Teilchen einzeln zu betrachten, deshalb werden statistische Werte eingeführt: die mittlere Geschwindigkeit der Teilchen, ihre Konzentration, die Masse des Teilchens. Die Formel, die den Zustand des Systems unter Berücksichtigung mikroskopischer Parameter charakterisiert, wird als Grundgleichung der molekularkinetischen Theorie der Gase (MKT) bezeichnet.
Ein wenig über die durchschnittliche Geschwindigkeit der Partikel
Die Bestimmung der Bewegungsgeschwindigkeit der Teilchen war zuerstwurde experimentell durchgeführt. Bekannt aus der Schulprogramm-Erfahrung, geleitet von Otto Stern, ließ sich eine Vorstellung von den Geschwindigkeiten von Teilchen erstellen. Im Verlauf des Experiments wurde die Bewegung von Silberatomen in rotierenden Zylindern untersucht: zunächst im stationären Zustand der Anlage, dann mit einer bestimmten Winkelgeschwindigkeit.
Als Ergebnis wurde festgestellt, dass die Geschwindigkeit der MoleküleSilber übersteigt die Schallgeschwindigkeit und beträgt 500 m / s. Die Tatsache ist ziemlich interessant, weil es schwierig ist, solche Geschwindigkeiten der Partikelbewegung in Substanzen zu erfassen.
Perfektes Gas
Fortsetzung der Forschung ist möglichNur in einem System, dessen Parameter durch direkte Messungen mit physikalischen Instrumenten bestimmt werden können. Die Geschwindigkeit wird mit einem Tachometer gemessen, aber die Idee, ein Tachometer an ein einzelnes Teilchen anzubringen, ist absurd. Man kann direkt nur die makroskopischen Parameter messen, die mit der Bewegung von Teilchen verbunden sind.

Jedes System von interagierenden Körperngekennzeichnet durch die potentielle Energie und kinetische Energie der Bewegung. Echtes Gas ist ein komplexes System. Variabilität potentieller Energie kann nicht systematisiert werden. Das Problem kann gelöst werden, indem ein Modell eingeführt wird, das die charakteristischen Eigenschaften des Gases trägt, wodurch die Komplexität der Wechselwirkung beseitigt wird.
Ideales Gas ist ein Zustand der Materie, in demdie Wechselwirkung der Teilchen ist vernachlässigbar, die potentielle Energie der Wechselwirkung neigt zu Null. Beträchtlich ist nur die Bewegungsenergie, die von der Geschwindigkeit der Teilchen abhängt.
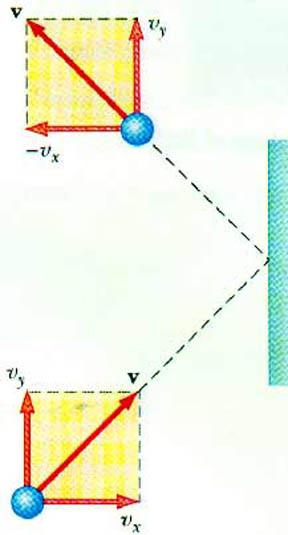
Der ideale Gasdruck
Identifizieren Sie die Beziehung zwischen Gasdruck und Geschwindigkeitseine Partikelbewegung ermöglicht Grundgleichung MKT ideales Gas. Ein Teilchen in einem Gefäß zu bewegen, bei der Kollision mit der Wand kann einen Impuls, dessen Wert überträgt es bestimmt werden, basierend auf II Newton'schen Gesetz:
- FΔt = 2 m0vx
Die Änderung des Impulses eines Teilchens in einem elastischen Stoß ist mit einer Änderung der horizontalen Komponente seiner Geschwindigkeit verbunden. F ist die Kraft, die für eine kurze Zeit t auf der Seite des Teilchens an der Wand wirkt; m0 Ist die Masse des Partikels.
Auf der Oberfläche S während der Zeit & Delta; t zugewandten Fläche alle Gasteilchen in Richtung der Oberfläche mit der Geschwindigkeit v bewegtenx und in einem Zylinder des Volumens Sv gelegenxΔt. Bei einer Partikelkonzentration n bewegt sich genau die Hälfte der Moleküle zur Wand, die zweite Hälfte - in die entgegengesetzte Richtung.
Nachdem wir die Kollision aller Teilchen betrachtet haben, können wir das Newtonsche Gesetz für die auf das Pad wirkende Kraft schreiben:
- FΔt = nm0vx2SΔt
Da der Gasdruck als das Verhältnis der Kraft definiert ist, wirkt die senkrecht zu der Oberfläche, kann der letzte Bereich geschrieben werden:
- p = F: S = nm0vx2
Die resultierende Beziehung als die grundlegende MKT-Gleichung kann das Gesamtsystem nicht beschreiben, da nur Bewegung in einer Richtung betrachtet wird.
Maxwell-Verteilung

Kontinuierliche häufige Kollisionen von Gaspartikeln mitWände und untereinander führen zur Etablierung einer gewissen statistischen Verteilung von Teilchen in Bezug auf Geschwindigkeiten (Energien). Die Richtungen aller Geschwindigkeitsvektoren erweisen sich als gleich wahrscheinlich. Diese Verteilung wurde als Maxwell-Verteilung bezeichnet. 1860 wurde dieses Muster von Maxwell auf der Basis des MKT abgeleitet. Die Hauptparameter des Verteilungsgesetzes sind die Geschwindigkeiten: wahrscheinlich, entsprechend dem maximalen Wert der Kurve, und der Effektivwert vQuadrat = √ <v2> Ist das mittlere Quadrat der Partikelgeschwindigkeit.
Eine Erhöhung der Gastemperatur entspricht einer Erhöhung des Wertes der Geschwindigkeiten.
Ausgehend von der Tatsache, dass alle Geschwindigkeiten gleich sind und ihre Module den gleichen Wert haben, können wir annehmen:
- <V2> = <Vx2> + <Vy2> + <Vz2>, Aus dem: <vx2> = <V2>: 3
Die grundlegende MKT-Gleichung, die den Durchschnittswert des Gasdrucks berücksichtigt, ist:
- p = nm0<V2>: 3.
Diese Beziehung ist insofern einzigartig, als sie die Beziehung zwischen mikroskopischen Parametern bestimmt: Geschwindigkeit, Partikelmasse, Partikelkonzentration und Gasdruck als Ganzes.
Unter Verwendung des Konzepts der kinetischen Energie von Teilchen kann die grundlegende MKT-Gleichung auf andere Weise umgeschrieben werden:
- p = 2 nm0<V2>: 6 = 2n <Ezu>: 3
Der Gasdruck ist proportional zum Durchschnittswert der kinetischen Energie seiner Teilchen.
Temperatur
Es ist interessant, dass für eine unveränderte Menge an Gas inEin geschlossenes Gefäß kann mit dem Gasdruck und der durchschnittlichen Energie der Teilchenenergie verbunden sein. Die Messung des Drucks kann durch Messung der Energie der Partikel erfolgen.
Was soll ich tun? Welchen Wert kann man mit der kinetischen Energie vergleichen? Ein solcher Wert ist die Temperatur.


Universelle Temperaturskala
Interessanter unter dem Gesichtspunkt der Unabhängigkeit vonDie Eigenschaften des Arbeitsfluids können als Gasthermometer angesehen werden. Ihr Maßstab hängt nicht von der Art des verwendeten Gases ab. In solch einem Instrument können wir hypothetisch die Temperatur identifizieren, bei der der Gasdruck gegen Null tendiert. Berechnungen zeigen, dass dieser Wert -273,15 entspricht oC. Die Temperaturskala (absolute Temperaturskala oder die Kelvin-Skala) wurde im Jahr 1848 Jahr eingeführt. Für den Hauptpunkt dieser Skala nahm nullten Gasdruck möglich Temperatur. Skaleneinheit Intervall gleich dem Einheitswert Celsius. Nimm Grundgleichung ILC Temperatur unter Verwendung ist bequeme Gas Prozesse in dem Studium.
Druck- und Temperaturbeziehung
Experimentell kann man die Proportionalität des Gasdrucks zu seiner Temperatur überprüfen. Gleichzeitig wurde festgestellt, dass der Druck direkt proportional zur Partikelkonzentration ist:
- P = nkT,
wo T die absolute Temperatur ist, ist k ein konstanter Wert gleich 1,38 · 10-23J / K.
Der Grundwert, der für alle Gase einen konstanten Wert hat, heißt Boltzmann-Konstante.
Vergleicht man die Abhängigkeit des Drucks von der Temperatur und die Grundgleichung der MKT-Gase, so können wir schreiben:
- <Ezu> = 3kT: 2
Der Durchschnittswert der kinetischen Bewegungsenergie von Gasmolekülen ist proportional zu seiner Temperatur. Das heißt, die Temperatur kann als Maß für die kinetische Energie der Teilchenbewegung dienen.







